如图a所示,水平桌面的左端固定一个竖直放置的光滑圆弧轨道,圆弧轨道底端与水平桌面相切C点,桌面CD长L=1m,高h2=0.5m,有质量为m(m为末知)的小物块从圆弧上A点由静止释放,A点距桌面的高度h1=0.2m,小物块经过圆弧轨道底端滑到桌面CD上,在桌面CD上运动时始终受到一个水平向右的恒力F作用.然后从D点飞出做平抛运动,最后落到水平地面上.设小物块从D点飞落到的水平地面上的水平距离为x,如图b是x2-F的图象,取重力加速度g=10m/s2.
(1)试写出小物块经D点时的速度vD与x的关系表达式;
(2)小物体与水平桌面CD间动摩擦因数μ是多大?
(3)若小物体与水平桌面CD间动摩擦因数μ是从第(2)问中的μ值的一半,再将小物块从A由静止释放,经过D点滑出后的水平位移大小为1m,求此情况下的恒力F的大小?
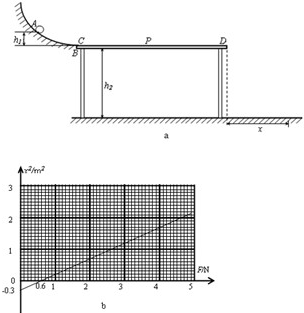
(1)物体从D滑出后做平抛运动,
水平方向x=vDt,竖直方向:h2=
gt2,1 2
解得vD=x
=g 2h2
x;10
(2)从A到D过程中,由动能定理得:
mgh1+FL-fL=
mvD2-0,1 2
f=μFN2=μmg,
x2=
F+4h2(h1-μL),4Lh2 mg
解得b=4h2(h1-μL),
由图象可知b=-0.3,解得μ=0.35,
(3)由(2)可知,k=
,4Lh2 mg
由图象可知k=0.5,解得m=0.4kg,
从A到D过程,由动能定理得:
mgh1+FL-
L=f+0 2
mvD2-0,1 2
由题可知:x=1m,
由第(1)问知vD=x
,g 2h2
解得:F=1.9N;

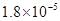 ,Ka(HSCN)=0.13;难溶电解质的溶度积常数:Kap(CaF2)=
,Ka(HSCN)=0.13;难溶电解质的溶度积常数:Kap(CaF2)=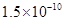
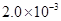 mol·L-1氢氟酸水溶液中,调节溶液pH(忽略体积变化),得到c(HF)、c(F-)与溶液pH的变化关系,如下图所示:
mol·L-1氢氟酸水溶液中,调节溶液pH(忽略体积变化),得到c(HF)、c(F-)与溶液pH的变化关系,如下图所示: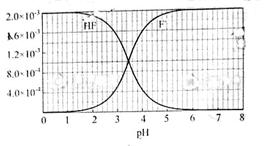
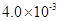 mol·L-1HF溶液与
mol·L-1HF溶液与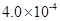 mol·L-1 CaCl2溶液等体积混合,调节混合液pH为4.0(忽略调节混合液体积的变化), (填“有”或“无”)沉淀产生。
mol·L-1 CaCl2溶液等体积混合,调节混合液pH为4.0(忽略调节混合液体积的变化), (填“有”或“无”)沉淀产生。