问题
选择题
反应①、②分别是从海藻灰和智利硝石中提取碘的主要反应:
①2NaI+MnO2+3H2SO4=2NaHSO4+MnSO4 +2H2O+I2
②2NaIO3+5NaHSO3=2Na2SO4+3NaHSO4+H2O+I2
下列说法正确的是
A.两个反应最终都能使溶液的酸性增强
B.碘元素在反应①中被还原,在反应②中被氧化
C.氧化性:MnO2>SO42—>IO3—>I2
D.反应①、2中生成等量I2时转移电子数之比为1:5
答案
答案:D
本题考查氧化还原反应.
反应①2NaI+MnO2+3H2SO4=2NaHSO4+MnSO4 +2H2O+I2中,反应物中有H2SO4这种强酸,而生成物中NaHSO4是种酸式盐,因而反应后酸性是降低的,故A错
反应①2NaI+MnO2+3H2SO4=2NaHSO4+MnSO4 +2H2O+I2中,NaI中的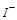 变成的
变成的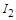 ,其化合价升高,碘元素被氧化,因而B错;
,其化合价升高,碘元素被氧化,因而B错;
在反应①中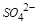 在反应前后各元素的化合价均无变化,因而没有体现其氧化还原的特性,因而C错误;
在反应前后各元素的化合价均无变化,因而没有体现其氧化还原的特性,因而C错误;
反应①中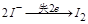 ,生成
,生成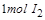 需转移电子数为
需转移电子数为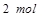 ;反应②中,
;反应②中,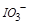 的碘的化合价为
的碘的化合价为 ,所以
,所以 ,生成
,生成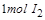 需转移电子数为
需转移电子数为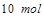 ;故生成等量的时转移电子数之比为
;故生成等量的时转移电子数之比为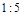 .
.
故正确答案为D
