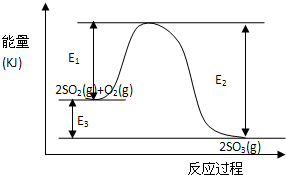
利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤.T℃时反应2SO2(g)+O2(g)AUTOTEXT<=>\*MERGEFORMAT 错误!未找到引用源.2SO3(g)过程中的能量变化如图所示,回答下列问题.
(1)T℃时将3molSO2和1molO2通入体积为2L的恒温恒容密闭容器中,发生反应.2min时反应达到平衡,此时测得反应物O2还剩余0.1mol,则达到平衡时SO2的转化率为 .
(2)下列叙述能证明该反应已达化学平衡状态的是 (填序号)
①SO2的体积分数不再发生变化 ②容器内压强不再发生变化 ③容器内气体分子总数不再发生变化 ④相同时间内消耗2n molSO2的同时生成n molO2 ⑤相同时间内消耗2n molSO2的同时生成2n molSO3
(3)反应 (填“放出”或“吸收”) 热量(用E1、E2或E3表示).
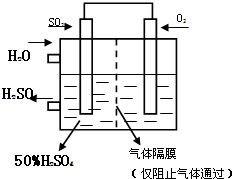
(4)若以右图所示装置,用电化学原理生产硫酸,将SO2、O2以一定压强喷到活性电极上反应.写出两电极的电极反应式: ; .为稳定持续生产,硫酸溶液的浓度应维持不变,则通入SO2和水的质量比为 .
(1)2SO2(g)+O2(g)⇌2SO3(g)
开始 3 mol 1mol 0
转化 1.8 mol 0.9mol 1.8 mol
平衡 1.2mol 0.1mol 1.8 mol
所以SO2的转化率=
×100%=60%1.8mol 3mol
故答案为:60%
(2)该反应前后气体体积减小,化学平衡状态的标志:正逆反应速率相等(同种物质)或正逆速率之比等于化学计量数之比(不同物质),反应混合物各组分的浓度不变、物质的量不变、含量为定值.
①②③④符合条件;⑤所指方向一致,故⑤错.
故选:①②④
(3)从图象知,反应物的能量大于生成物的能量,所以该反应是放热反应;
根据能量守恒放出的热量为E3 或E2-E1.
故答案为:放热;E3 或E2-E1
(4)该原电池的本质是2SO2+O2+2H2O=2H2SO4,SO2在负极上发生氧化反应电极反应式为SO2-2e-+2H2O═SO42-+4H+,O2在正极上发生还原反应电极反应式为O2+4e-+4H+═2H2O;
为维持浓度不变,SO2和O2、H2O反应生成硫酸的质量分数是50%,所需的水为反应的水和做溶剂的水,所以质量比为=2×64:(2×18+2×98)=16:29
故答案为:正极:O2+4e-+4H+═2H2O,负极:SO2-2e-+2H2O═SO42-+4H+; 16:29
