问题
计算题
黄铜矿(主要成分CuFeS2)是提取铜的主要原料
(1)取12.5g黄铜矿样品,经测定含3.60g硫(杂质不含硫),矿样中CuFeS2含量为
(2)已知产物Cu2S在1200℃高温下班继续反应:
2Cu2S + 3 O2 → 2Cu2O + 2 SO2
2Cu2O + Cu2S → 6Cu + SO2
假定各步反应都完全,完成下列计算:
①由6 mol CuFeS2生成6 mol Cu,求消耗O2的物质的量
②6 mol CuFeS2和14.25 mol O2反应,理论上可得到多少摩尔铜
③6 mol CuFeS2和15.75 mol O2反应,理论上可得到多少摩尔铜
答案
(1)82.8%
(2)①CuFeS2 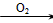 Cu+FeO+2SO2
Cu+FeO+2SO2
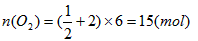
② O2不是量 Cu2S+O2 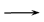 2Cu+SO2
2Cu+SO2
n(Cu)=6-2(15-14.25)= 4.5 (mol)
③O2过量 2Cu2S+3O2 → 2Cu2O+2SO2
n(Cu)=6(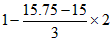 )=3 (mol)
)=3 (mol)
