问题
计算题
将一充满NO2和O2混合气体的试管倒立于水中,若试管的容积为10 mL,充分反应后剩余气体为1 mL,求原混合气体中NO2和O2的体积各为多少毫升?
答案
(1)若O2过量,剩余的1 mL气体为O2。
根据4NO2+O2+2H2O=4HNO3,
得:V(NO2)=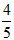 ×9 mL =7.2 mL,
×9 mL =7.2 mL,
V'(O2)=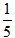 ×9 mL =1.8 mL。
×9 mL =1.8 mL。
故V(O2) =1.8 mL+1 mL=2.8 mL。
(2)若NO2过量,剩余的1 mL气体为NO。
先根据3NO2+H2O=2HNO3+NO得出过量的NO2体积为3 mL。
再根据4NO2+O2+2H2O=4HNO3
计算参加反应的NO2.O2的体积:
V'(NO2)=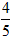 ×7 mL =5.6 mL,
×7 mL =5.6 mL,
V(O2)=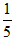 × 7 mL= 1.4 mL。
× 7 mL= 1.4 mL。
故V(NO2)=5.6 mL+3 mL= 8.6 mL,V(O2)= 1.4 mL。
