问题
填空题
为妥善处理氯甲烷生产企业的副产物CCl4,以减少其对臭氧层的破坏,化学家研究在催化条件下,通过下列反应,使CCl4转化为重要的化工原料氯仿(CHCl3)。 CCl4+H2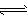 CHCl3 +HCl 此反应伴随有副反应,会生成CH2Cl2、CH3Cl和CH4等。已知CCl4的沸点为77℃,CHCl3的沸点为61.2℃。在密闭容器中,该反应达到平衡后,测得如下数据(假设不考虑副反应)。
CHCl3 +HCl 此反应伴随有副反应,会生成CH2Cl2、CH3Cl和CH4等。已知CCl4的沸点为77℃,CHCl3的沸点为61.2℃。在密闭容器中,该反应达到平衡后,测得如下数据(假设不考虑副反应)。

①此反应在110℃时平衡常数为____。
②实验1中,CCl4的转化率A____50%(填“大于”、“小于”或“等于”)。
③实验2中,10h后达到平衡,H2的平均反应速率为____。在此实验的平衡体系中,再加入0.5mol CCl4和1.0mol HCl,平衡将向___反应方向移动。
④实验3中,B的值___(选填序号)。
A.等于50%
B.大于50%
C.小于50%
D.从本题资料,无法判断
答案
①1
②大于
③0. 05mol·L-1·h-1; 逆
④D
