问题
填空题
工业生产硫酸时,将SO2催化氧化转化为SO3是关键步骤。
(1)已知每生成1 mol 气态SO3放出98.3kJ的热量,该反应的热化学方程式是:__________________。
(2)实际生产中,SO2的催化氧化采用400°C-500°C和常压,结合下面数据回答问题:压强及温度对SO2的转化率如下表(原料气各成分体积分数为SO2 7%,O2 11%,N2 82%)
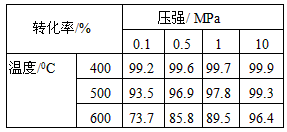
①根据表中数据推断并阐述SO2的氧化是放热过程_______________________
②在400°C时,当平衡状态由0.5 MPa变到1 MPa时,平衡常数K(0.5MPa)_______K(1MPa)(填>、<、=)。
③工业生产中,SO2的催化氧化采用常压,而不是高压,其主要原因是___________,____________。
④下列变化不能提高SO2转化率的是________。
a.增大压强 b.使用催化剂 c.升高温度 d.增加O2的浓度
答案
(1)2SO2(g) + O2(g)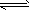 2SO3(g) ΔH=-196.6kJ/mol
2SO3(g) ΔH=-196.6kJ/mol
(2)①压强相同时温度越高二氧化硫转化率越低,即升温平衡向逆反应方向移动,逆反应吸热,正反应放热;
②=;
③ 在400℃-500℃时,增大压强,二氧化硫的转化率增大不够显著,且增大压强对设备的要求高,所以常压即可;
④b
