问题
计算题
已知①H2(g)+Cl2(g)====2HCl(g)ΔH1="-184.6" kJ·mol-1,则②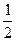 H2(g)+
H2(g)+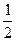 Cl2(g)="===HCl(g)" ΔH2="-x" kJ·mol-1中的x的值是多少?
Cl2(g)="===HCl(g)" ΔH2="-x" kJ·mol-1中的x的值是多少?
答案
x的值为92.3
由于反应②中各物质的化学计量数是反应①中各物质的化学计量数的一半,所以,反应热也该是一半。那么x=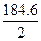 =92.3。
=92.3。
已知①H2(g)+Cl2(g)====2HCl(g)ΔH1="-184.6" kJ·mol-1,则②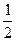 H2(g)+
H2(g)+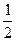 Cl2(g)="===HCl(g)" ΔH2="-x" kJ·mol-1中的x的值是多少?
Cl2(g)="===HCl(g)" ΔH2="-x" kJ·mol-1中的x的值是多少?
x的值为92.3
由于反应②中各物质的化学计量数是反应①中各物质的化学计量数的一半,所以,反应热也该是一半。那么x=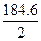 =92.3。
=92.3。