问题
填空题
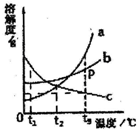
图为a、b、c三种物质的溶解度曲线.请根据溶解度曲线回答下列问题:
(1)点P是物质b在t3℃时曲线上的一点.该点是b物质的______(填“饱和”或“不饱和”,下同)溶液,是a的______溶液
(2)t2℃,欲配制等质量的a、b、c三种物质的饱和溶液,所需水的质量大小关系是______
(3)若将t3℃时的a、b、c三种饱和溶液降温到t1℃,则t1℃时三种溶液的溶质质量分数由大到小的顺序是______
(4)现将混有少量c的a溶液进行提纯,最好的方法是______.
答案
(1)在溶解度曲线上的点表示饱和溶液,在曲线以下的点表示不饱和溶液,故答案为:饱和;不饱和;
(2)同温度下,不同物种的等质量的饱和溶液,溶解度越大,含有的水越多,所以t2℃时a、b、c三种物质的溶解度大小为:b>a=c,所含水的多少为:a=c>b,故答案为:a=c>b;
(3)饱和溶液的质量分数的计算方法是:
×100%,因为t1℃时a、b、c的溶解度大小是:a>b>c所以t3℃时a、b、c的饱和溶液的质量分数是a>b>c,降温后a和b都析出晶体,仍然是饱和溶液,又因为t1℃时,b的溶解度大于a的,所以t3℃时,b的饱和溶液的质量分数大于a物质的饱和溶液的质量分数;由于c物质降温后变为不饱和溶质质量分数不变,所以要比较c物质在t3℃时的溶解度与t1℃时a和b物质的溶解度大小,通过图表可知:b>c>a.溶解度 100g+溶解度
(4)a物质的溶解度随温度升高而增大,而c物质的溶解度随温度升高而降低,所以可以通过降温使a物质析出(c物质不会析出)而得到纯净的a物质.
故答案为:降温结晶;