如图是A、B、C三种物质的溶解度曲线,据图回答:
(1)t2℃时A、B、C三种物质的溶解度由大到小的顺序是______
(2)t1℃时30gA物质加入到50g水中不断搅拌,形成的溶液质量是______g.
(3)将t2℃时A、B、C三种物质都是60g的饱和溶液(溶液中 均无晶体剩余)的温度降到t1℃时,此时三种溶液的溶质质量分数由大到小关系是______>______>______;此时所得溶液质量大小关系是______>______>______.
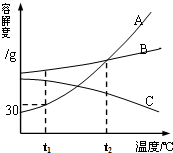
(1)t2℃时A、B、C三种物质的溶解度由大到小的顺序是A=B>C;
(2)t1℃时A的溶解度是30g,即100g水中最多溶解30gA,所以30gA物质加入到50g水中不断搅拌,形成的溶液质量是65g;
(3)A、B的溶解度随温度的降低而减小,C的溶解度随温度的降低而增大,所以若将t2℃时的A、B、C三种物质的饱和溶液降温至t1℃,AB会析出晶体,C变为不饱和溶液,溶质的质量分数与t2℃时相同;饱和溶液中溶质的质量分数的计算式
×100%,可知溶解度越大质量分数也就越大,降温至t1℃时B的溶解度大于A,A的溶解度小于t2℃时C的溶解度,所以此时溶液中溶质质量分数由大到小的顺序为B>C>A;所以将t2℃时A、B、C三种物质都是60g的饱和溶液(溶液中 均无晶体剩余)的温度降到t1℃时,此时三种溶液的溶质质量分数由大到小关系BCA,C无溶质析出,则溶液质量不变,A的溶解度变化大,析出晶体多,则剩余溶液质量小;溶解度 100g+溶解度
故答案为:(1)A=B>C;(2)65;(3)BCA;CBA.
