(15分)在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂过氧化氢,当它们混合时,即产生大量氧气和水蒸气,并放出大量热。已知0.4mol液态肼与足量过氧化氢反应,生成氮气和水蒸气,放出256.65kJ的热量。
(1)写出肼和过氧化氢的电子式:肼___________________,过氧化氢______________ 。
(2)写出该反应热化学方程式:________________________________________________。
(3)已知H2O(1)==H2O(g) △H=+44kJ/mol,则16g液态肼与足量液态过氧化氢反应生成氮气和液态水时,放出的热量是_____________________ kJ。
(4)上述反应用于火箭推进剂,除释放大量热和快速产生大量气体外,还有一个很突出的优点是:_____________________________________________________________________。
(1)略
(2)N2H4(l)+2 H2O2(l)= N2(g)+ 4H2O(l)△H=-641.625KJ/mol
(3)400.8KJ
(4) 无污染
⑴肼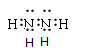 过氧化氢
过氧化氢
(2)1molN2H4放热=256.65kJ×1mol/0.4mol=641.625kJ
N2H4(l)+2 H2O2(l)= N2(g)+ 4H2O( g)△H=-641.625KJ/mol
⑶N2H4(l)+2 H2O2(l)= N2(g)+ 4H2O( g)△H=-641.625KJ/mol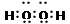 与H2O(1)==H2O(g) △H=+44kJ/mol乘以4相减得N2H4(l)+2 H2O2(l)= N2(g)+ 4H2O(l)△H=-801.6KJ/mol,则16gN2H4为0.5mol, 放出的热量是400.8KJ ;⑷产物为N2和H2O无污染。
与H2O(1)==H2O(g) △H=+44kJ/mol乘以4相减得N2H4(l)+2 H2O2(l)= N2(g)+ 4H2O(l)△H=-801.6KJ/mol,则16gN2H4为0.5mol, 放出的热量是400.8KJ ;⑷产物为N2和H2O无污染。
