若不慎发生砒霜泄露,应急的措施是采用石灰中和,使被污染的河水含砷量降低到国家允许的标准范围内,以消除可能会造成的危害。测定砷是利用下述反应:AsO33- + I2 + H2O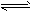 AsO43- + 2I- +2H+ 这反应是可逆的,控制溶液的酸碱性,可以测定不同价态(+3或+5)的砷。今有一试样,含As2O3的As2O5及其它对测定没有影响的杂质。将此试样用NaOH溶液溶解后,在中性溶液中用0.02000mol·L-1的I2-KI溶液滴定,用去25.00mL。滴定完毕后,使溶液呈酸性,加入过量的KI。由此析出的碘又用0.1250mol·L-1的
AsO43- + 2I- +2H+ 这反应是可逆的,控制溶液的酸碱性,可以测定不同价态(+3或+5)的砷。今有一试样,含As2O3的As2O5及其它对测定没有影响的杂质。将此试样用NaOH溶液溶解后,在中性溶液中用0.02000mol·L-1的I2-KI溶液滴定,用去25.00mL。滴定完毕后,使溶液呈酸性,加入过量的KI。由此析出的碘又用0.1250mol·L-1的
Na2S2O3溶液滴定,用去24.00 mL。试计算试样中As2O3和As2O5的质量。(已知2Na2S2O3 + I2=Na2S4O6+ 2NaI)
n(I2)=0.0200 mol·L-1×0.025L=0.000500mol
I2~AsO33-~1/2As2O3
n(As2O3)=0.000500mol÷2=0.000250mol
m(As2O3)=0.000250mol×198 g·mol-1=0.0495g
n(Na2S2O3)=0.125 mol·L-1×0.0240L=0.00300mol
Na2S2O3~1/2I2~1/2AsO43-
n(AsO43-)=0.00300mol÷2=0.00150mol
n(As2O5)=(0.00150mol-0.000500mol)÷2=0.000500mol
m(As2O5)=0.000500mol×230 g·mol-1=0.115g
