问题
填空题
(1)用“双线桥”表示电子转移的方向和数目:3NO2+H2O=2HNO3+NO
如果此反应过程中转移电子数为4mol,则生成的硝酸的物质的量为______mol.
(2)用“单线桥”表示电子转移的方向和数目:2KMnO4+16HCl(浓)=2KCl+2MnCl2 +5Cl2↑+8H2O
氧化剂为______,如果此反应生成5mol Cl2,发生氧化反应的HCl的物质的量为______mol.
答案
(1)反应二氧化氮中氮元素化合价既升高也降低,二氧化氮既作氧化剂又作还原剂,3mol的NO2中,2mol做还原剂,1mol做氧化剂,转移的电子为2mol,
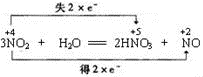
,即3mol的NO2反应,生成2mol硝酸转移2mol电子,转移电子数为4mol,则生成的硝酸的物质的量为4mol,
故答案为:

;4;
(2)反应的氧化剂是高锰酸钾,还原剂是盐酸,在反应的16mol盐酸中,只有10mol做还原剂,被氧化、发生氧化反应,同时转移电子是10mol,用单线桥表示反应中电子转移的方向和数目为
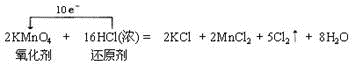
,
故答案为:
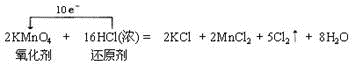
;KMnO4;10.
