(12分)按要求完成各题
(1)已知,1mol N2(g)与足量O2(g)起反应,生成2mol NO2(g),吸收68 kJ的热量。该反应的热化学方程式可表示为:
(2)写出下列各物质的电离方程式:
CH3COOH
NH3·H2O
 (3)写出下列各物质水解的离子方程式:
(3)写出下列各物质水解的离子方程式:
NaHCO3
AlCl3
(4)把足量的碳酸钙粉末放入水中,建立的溶解平衡可表示为:
(1)N2(g) + 2O2(g)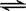 2NO2(g) △H = +68kJ/mol
2NO2(g) △H = +68kJ/mol
(2) CH3COOH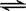 CH3COO- + H+ NH3·H2O
CH3COO- + H+ NH3·H2O 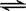 NH4+ + OH-
NH4+ + OH-
(3) HCO3- + H2O 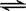 H2CO3 + OH- Al3+ + 3H2O
H2CO3 + OH- Al3+ + 3H2O 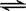 Al(OH)3 + 3H+
Al(OH)3 + 3H+
(4) CaCO3(S) 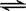 Ca2+ (aq) + CO32- (aq)
Ca2+ (aq) + CO32- (aq)
(1)考查热化学方程式的书写。需要注意的是要标出各物质的状态,反应热的数值、符号和单位;(2)考查电离方程式的书写。要注意分清是强电解质还弱电解质,强电解质用等号,弱电解质用可逆号。如果是多元弱酸还要分布电离;(3)在书写水解方程式时要用可逆号,一般不标“↑”或“↓”。如果是多元弱酸根还要分布水解;(4)溶解平衡方程式的书写要标出状态,用可逆号。
