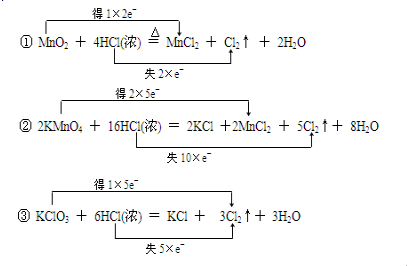
(1)实验室常用以下几种方法制取氯气,用双线桥标出电子转移方向和数目
①MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O △ .
②2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
③KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O
(2)用浓盐酸来制取Cl2 时,当参加反应的HCl 为146g时,用______反应(填①②③)
(3)可制得最多的氯气,并根据该反应列式计算在标准状况下可制得多少升氯气?被氧化的物质的质量是多少克?
(1)MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,该反应中MnO2→MnCl2,Mn元素由+4价→+2价,一个MnO2分子失去2个电子; HCl(浓)→Cl2,Cl元素由-1价→0价,生成一个Cl2分子需2个 HCl分子失去2个电子,所以得失电子最小公倍数为2; △ .
2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,该反应中KMnO4→MnCl2,Mn元素由+7价→+2价,一个KMnO4分子得到5个电子,HCl(浓)→Cl2,Cl元素由-1价→0价,生成一个Cl2分子需2个 HCl分子失去2个电子,所以得失电子最小公倍数为10;
KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O,该反应中KClO3→Cl2,Cl元素由+5价→0价,一个KClO3分子得5个电子,HCl(浓)→Cl2,Cl元素由-1价→0价,一个HCl分子失去一个电子,所以得失电子最小公倍数为5.
故答案为:
;
(2)把下列方程式换成HCl的计量数一样的方程式,比氯气的计量数大小,计量数大的生成的氯气多.
①4MnO2+16HCl(浓)
4MnCl2+4Cl2↑+8 H2O △ .
②2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
③
KClO3+16HCl(浓)=8 3
KCl+8Cl2↑+8H2O8 3
通过比较得,相同的浓盐酸参加反应③可制得最多的氯气.
故答案为:③.
(3)设生成氯气的体积为x,
③KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O
219g 67.2L
146g x
x=
=44.8L67.2L×146g 219g
又有6molHCl参加反应有 5mol被氧化,设有y被氧化.
6HCl------5HCl
(36.5×6)g (36.5×5)g
146g y
y=
=121.7g(36.5×5)g×146g (36.5×6)g
答:在标准状况下可制得氯气44.8L,被氧化的物质的质量为121.7g.
