问题
选择题
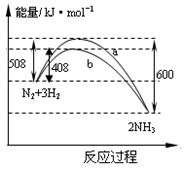
下图表示298K时N2与H2反应过程中的能量变化。根据下图叙述正确的是( )
A.该反应的热化学方程式为:1/2 N2(g)+3/2 H2(g) NH3(g) △H= -92kJ·mol-1
NH3(g) △H= -92kJ·mol-1
B.不用催化剂,生成 1molNH3放出的热量为46 KJ
C.加入催化剂,生成 1molNH3的反应热减小50 KJ·mol-1
D.曲线b表明加入催化剂降低了反应热,加快了反应速率
答案
答案:B
由图知:N2(g)+3 H2(g) 2NH3(g) △H= -92kJ·mol-1;催化剂只能改变反应的历程,并不会改变反应热的大小。
2NH3(g) △H= -92kJ·mol-1;催化剂只能改变反应的历程,并不会改变反应热的大小。
