问题
填空题
过氧化氢(H2O2)有广泛的用途。工业上用电解硫酸氢铵水溶液的方法制备过氧化氢,其反应原理是:
2NH4HSO4 (NH4)2S2O8+H2↑,(NH4)2S2O8+2H2O==2NH4HSO4+H2O2。其流程如下
(NH4)2S2O8+H2↑,(NH4)2S2O8+2H2O==2NH4HSO4+H2O2。其流程如下
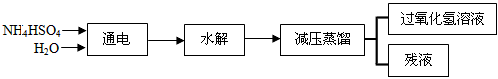
回答下列问题:
(1)根据以上反应原理可知,电解硫酸氢铵溶液时,阳极的电极反应方程式是:_________________。
(2)在上流程图中,采用减压蒸馏的原因是:______________。可循环利用的物质是______________。
(3)过氧化氢具有的化学性质是________________。
A.不稳定性 B.弱碱性 C.氧化性 D.还原性
(4)硫酸铜酸性溶液中混有少量硫酸亚铁,为除去杂质,用过氧化氢把硫酸亚铁氧化,反应的离子方程式是_________________________________________________。
(5)在硫酸的存在下,用过氧化氢与乙酸作用制备过氧乙酸(CH3COOOH)的化学方程式是:_________________________________。
答案
(1)2SO42--2e-==S2O82-
(2)过氧化氢不稳定,受热容易分解,减小气压,使液体沸点降低;残液(NH4HSO4溶液)
(3)ACD
(4)2Fe2++H2O2+2H+==2Fe3++2H2O
(5)CH3COOH+H2O2 CH3COOOH+H2O
CH3COOOH+H2O
