问题
填空题
锂被誉为“高能金属”。工业上用硫酸与β-锂辉矿(LiAlSi2O6和少量钙镁杂质)在一定条件下反应生成Li2SO4(以及MgSO4、硅铝化合物等物质),进而制备金属锂,其生产流程如下
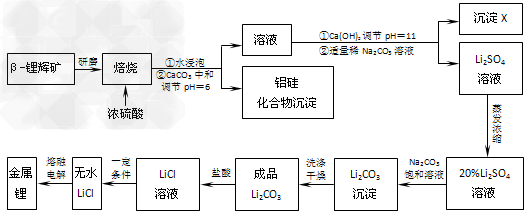
(1)用氧化物形式表示LiAlSi2O6的组成:________________ 。
(2)沉淀X主要成分为CaCO3和___________。
(3)写出盐酸与Li2CO3反应的离子方程式:___________________。
(4)写出电解熔融LiCl时阴极的电极反应式:__________________。
(5)流程中两次使用了Na2CO3溶液,试说明前后浓度不同的原因:前者是____________;后者是_________________。
答案
(1)Li2O·Al2O3·4SiO2
(2)Mg(OH)2
(3)Li2CO3+2H+=2Li++ H2O+CO2↑
(4)Li++ e-=Li
(5)浓度过大会使部分Li+ 沉淀;此时浓度大则有利于Li2CO3沉淀的生成
