抗战时期中国老百姓用硝土和草木灰制出KNO3后,再与硫和木炭混合制造了大量土地雷,炸得日本鬼子魂飞魄散.(6分)
 (1)硝土的主要成分是NaNO3,和Ca(NO3) 2等,将其加水溶解除去不溶物后,加入适量的草木灰(主要成分是K2CO3),若恰好完全反应,则生成CaCO3沉淀的反应方程式为________________________,其反应类型是________.将CaCO3与溶液分离的操作是_________,所得溶液中的溶质是________和_________.
(1)硝土的主要成分是NaNO3,和Ca(NO3) 2等,将其加水溶解除去不溶物后,加入适量的草木灰(主要成分是K2CO3),若恰好完全反应,则生成CaCO3沉淀的反应方程式为________________________,其反应类型是________.将CaCO3与溶液分离的操作是_________,所得溶液中的溶质是________和_________.
(2)最后用冷却热饱和溶液结晶的方法从滤液
中得到其中一种晶体.据此判断:
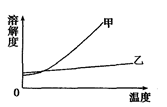
甲、乙两位同学绘制的该晶体的溶解度曲线
(见上图)较准确的是_________(填“甲”或“乙”).
分析:(1)根据复分解的原理和反应的条件,及固体和液体分离常用的方法来解答;
(2)根据常见的结晶的方法来解答.物质的溶解度随温度变化比较大者一般用冷却结晶的方法结晶.
解答:解:(1)根据所给的三种物质的分类都属于盐,故它们的反应属于复分解反应,所以能反应的为硝酸钙和碳酸钾,它们反应生成了碳酸钙沉淀,K2CO3+Ca(NO)3=KNO3+CaCO3↓,所以在分离时应该通过过滤操作来实现;
(2)根据题意是把溶液放入冰窟中得到了晶体,说明该固体的溶解度受温度变化较大,所以符合该条件的曲线为甲;
故答案为:(1)K2CO3+Ca(NO)3=KNO3+CaCO3↓;复分解;过滤;NaNO3;KNO3;
(2)甲.
