黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可以制备硫、铁和镍的化合物。
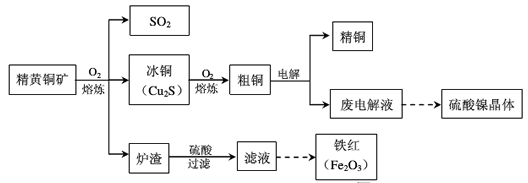
回答下列问题。
(1) Cu2S熔炼过程发生的主要反应为:
2Cu2S(s)+3O2(g)=2Cu2O(s)+2SO2(g) △H=-768.2 kJ/mol
2Cu2O(s)+Cu2S(s)=6Cu(s)+SO2(g) △H=+116.0 kJ/mol
在熔炼过程中不需要持续加热,原因是____。
(2)熔炼过程中产生大量的___(填分子式),可进一步加工并作为上述流程中的原料加以循环利用。
(3)炉渣的主要成分是Fe2O3、FeO、Al2O3、SiO2,为了得到铁红,需对上述滤液进行处理,处理过程涉及下列步骤中的___(填序号)。
A.氧化 B.还原 C.灼烧 D.加碱
(4)废电解液中含有较多的Ni2+ ,从废电解液提取硫酸镍晶体,需要用电解法把电解液中的Cu2+ 除去,电解的阳极可以采用___作为电极材料,阳极的电极反应式是____。
(5)从废电解液中除去Pb2+的方法是往其中通入H2S至饱和,使Pb2+转化为硫化铅沉淀,溶液的 pH对转化效果的影响是____。已知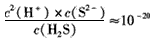 ,饱和H2S溶液中c( H2S)为0.1 mol/L,NiS的Ksp=10-11,若废 电解液的pH =5,为保证不生成NiS沉淀,Ni2+的浓度应控制在__以下。
,饱和H2S溶液中c( H2S)为0.1 mol/L,NiS的Ksp=10-11,若废 电解液的pH =5,为保证不生成NiS沉淀,Ni2+的浓度应控制在__以下。
(1)Cu2S与O2反应的热化学方程式为:Cu2S(s)+O2(g)=2Cu(s)+SO2(g) △H= - 217.4kJ/mol,反应放出的热量足以维持反应的进行
(2) SO2
(3)ACD
(4)惰性电极 ;4OH--4e-=2H2O+O2↑(或Ni - 2e - =Ni2+)
(5)溶液的pH越大,转化效果越好 ;1 mol/L
