在人生旅途上,得到是一种收获,经历是一种收获,体验是一种收获,成功是一种收获,甚至失败也是一种收获……
请以“我收获了 ”为题,写一篇文章。
略
题目分析:本篇作文是一篇半命题作文,“收获”是什么? 是成功、掌声、笑脸、鲜花、喜悦、敬佩、满足,还是经历、感悟、快乐或者忧伤?可写的内容很多,所提供的材料对我们的写作内容往往有提示、导向甚至限制的作用,所以我们不能忽视,应该对材料进行分析,提取观点。
点评:怎样写好一篇半命题作文?半命题作文就是命题人限定题目一部分的内容,学生根据要求将题目补充完整,然后再进行写作的作文命题形式。半命题作文的灵活度介于话题作文与全命题作文之间,对学生来说既有所限制又不失开放性,在立意、选材、构思等方面给考生适当的选择余地。半命题形式既有利于考生个性的张扬,又能较好地避免宿构和猜题押题,能较为真实地反映学生的写作水平。

 CO(g)+H2(g) ΔH=+131.3 kJ·mol-1,
CO(g)+H2(g) ΔH=+131.3 kJ·mol-1,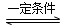 2NH3(g) ΔH=-92.4 kJ·mol-1。实验室模拟化工生产,分别在不同实验条件下反应,N2浓度随时间变化如图甲所示。
2NH3(g) ΔH=-92.4 kJ·mol-1。实验室模拟化工生产,分别在不同实验条件下反应,N2浓度随时间变化如图甲所示。