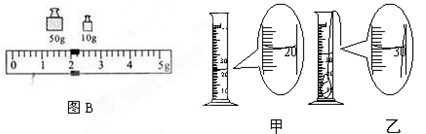
利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。
Ⅰ.用乙烯作为还原剂将氮的氧化物还原为N2是燃煤烟气的一种脱硝(除NOx)技术。其脱硝机理如下图1,脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如下图2所示。
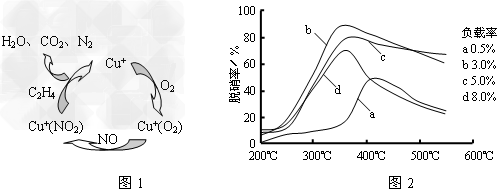
①写出该脱硝过程中乙烯和NO2反应的化学方程式____________________________。
②为达到最佳脱硝效果,应采取的条件是_______________。
Ⅱ.有学者设想以下图所示装置用电化学原理将燃煤烟气中的CO2、SO2转化为重要化工原料。
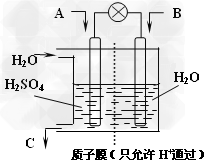
(1)若A为CO2,B为H2,C为CH3OH,则正极电极反应式为_______________。
(2)若A为SO2,B为O2,C为H2SO4。科研人员希望每分钟从C处获得100mL10mol/L
H2SO4,则A处通入烟气(SO2的体积分数为1%)的速率为______ L/min(标准状况)。
Ⅲ.粗CuO是将工业废铜、废电线及废铜合金高温焙烧而成的,杂质主要是铁的氧化物及泥沙。以粗CuO为原料制备CuSO4 5H2O的主要步骤如下图所示:
5H2O的主要步骤如下图所示:
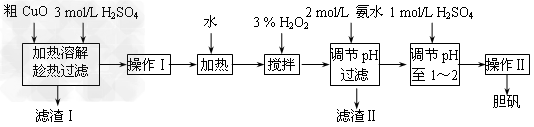
Fe3+、Fe2+、Cu2+转化为相应氢氧化物时,开始沉淀和沉淀完全时的pH如下表

(1)加入3 % H2O2之前需将热溶液冷却,其目的是____________,H2O2的作用是____________________________。
(2)加入2 mol/L氨水后,溶液的pH应在_____________范围内。
(3)经操作Ⅰ得到粗胆矾,经操作Ⅱ得到精制胆矾。两步操作相同,都包括______ 、过滤、洗涤、干燥等步骤。
Ⅰ.①2C2H4+6NO2=4CO2+3N2+4H2O [或2CH=CH2+6NO2→4CO2+3N2+4H2O]
②350℃(或340℃~360℃) 、负载率3%
Ⅱ.(1)CO2+6H++6e-=CH3OH+H2O;(2)2240
Ⅲ.(1)防止H2O2分解;将Fe2+氧化为Fe3+,使之在Cu2+之前沉淀;(2)3.2~4.7; (3)蒸发浓缩、冷却结晶