问题
填空题
高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺如下
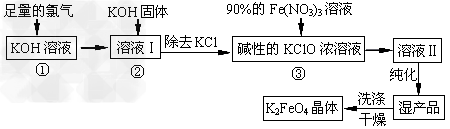
(1)反应①应在温度较低的情况下进行。因在温度较高时KOH与Cl2反应生成的是KClO3。写出在温度较高时KOH 与Cl2反应的化学方程式____________________,该反应的氧化产物是___________。
(2)在溶液I中加入KOH固体的目的是_________ (填编号)。
A.与溶液I中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供碱性的环境
D.使KClO3转化为 KClO
(3)从溶液II中分离出K2FeO4后,还会有副产品KNO3、KCl,则反应③中发生的离子反应方程式为___________________。
(4)如何判断K2FeO4晶体已经洗涤干净_________________。
(5)高铁酸钾(K2FeO4)作为水处理剂的一个优点是能与水反应生成胶体吸附杂质,配平该反应的离子方程式:___FeO42-+ ___H2O = ___Fe(OH)3(胶体)+ ___O2↑+ ___OH- 。
答案
(1)6KOH+3Cl2 KClO3+5KCl+3H2O;KClO3
KClO3+5KCl+3H2O;KClO3
(2)AC
(3)2Fe3+ + 3ClO- + 10OH- =2FeO42- + 3Cl-+ 5H2O
(4)用试管取少量最后一次的洗涤液,加入硝酸银溶液,无白色沉淀则已被洗净
(5)4、10、4、3、8
