问题
填空题
(12分)氯化铍是用于制有机铍化合物和金属铍的重要原料。
(1)BeCl2分子中组成元素Be的基态原子的价电子排布式为 ,其元素的第一电离能 B元素(填“>”或“<” 或“=”),原因是 。
(2)已知BeCl2加热易升华,液态BeCl2不导电,BeCl2晶体类型为 ; BeCl2中Be原子的杂化轨道类型是 。
(3)用阴离子树脂交换法提取一种组成元素为氯和铍的阴离子,该阴离子内铍原子达到8电子稳定结构,则该离子内存在的微粒间的作用力是 ,阴离子的结构式为 。
答案
(1)2s2 (2分); > (1分); Be的2s轨道全充满,体系能量低(2分)。
(2)分子晶体(1分); sp (2分)
(3)共价键和配位键 (2分) ; 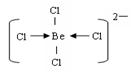 (2分)
(2分)
(1)Be是第ⅡA元素,所以根据构造原理可知,Be原子的基态价电子排布式为2s2。非金属性越强,第一电离能越大,但由于Be的2s轨道全充满,稳定性强,体系能量低,所以第一电离能大于B的。
(2)根据BeCl2的物理性质可判断,形成的晶体应是分子晶体、BeCl2分子中心原子没有孤对电子,所以是直线型结构,采用sp杂化。
(3)阴离子内铍原子达到8电子稳定结构,说明分子内除了含有共价键以外,还一定存在配位键,即氯原子提供电子对,Be原子提供空轨道,结构式为 。
。
