下图是A、B、C三种固体物质的溶解度曲线,试回答下列问题:

(1)t3℃三种物质的溶解度由大到小的顺序为: ▲ 。
(2)现有一杯20℃接近饱和的溶液,温度升高到40℃时,变为饱和溶液,你认为该物质可能是A、B、C中的 ▲ 。
(3)将t3℃A、B、C的饱和溶液分别降温到t1℃,此时所得溶液中溶质的质量分数由大到小的顺序是__________▲__________。
(4)当A中混有少量B时,我们可以采用_________▲_________法,提取较纯净的A。
(1)A>B>C (2)C (3)B>C>A
(4)降温结晶(或冷却热饱和溶液)
本题考查的是固体溶解度曲线及其作用;,混合物的分离方法;结晶的原理、方法及其应用。固体的溶解度是指在一定的温度下,某固体物质在100克溶剂中达到饱和状态时所溶解的质量。根据固体物质的溶解度曲线可知:①查出某固体物质在某温度下的溶解度,②比较不同的物质在同一温度下溶解度的大小,③判断物质的溶解度随温度变化的变化情况,④判断通过降温还是蒸发溶剂的方法达到结晶的目的等。
(1)t3℃三种物质的溶解度从上到下依此变小,故A>B>C;
(2)从20℃升到40℃,A、B两物质的溶解度变大,不会由接近饱和的溶液变成饱和溶液,C物质溶解度变小,有可能由接近饱和的溶液变成饱和溶液;
(3)将t3℃A、B、C的饱和溶液分别降温到t1℃,A、B溶解度变小,有晶体析出,A、B仍为饱和溶液,故可用此温度下的溶解度计算其饱和溶液的溶质质量分数,即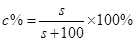 ,由此时SA﹤SB,所以A的溶质质量分数小于B;将t3℃A、B、C的饱和溶液分别降温到t1℃时,C溶解度变大,C成为不饱和溶液,但溶质质量分数没变,应等于其在t3℃时的饱和溶液的溶质质量分数,依据上面的公式,则有B>C>A;
,由此时SA﹤SB,所以A的溶质质量分数小于B;将t3℃A、B、C的饱和溶液分别降温到t1℃时,C溶解度变大,C成为不饱和溶液,但溶质质量分数没变,应等于其在t3℃时的饱和溶液的溶质质量分数,依据上面的公式,则有B>C>A;
(4)当A中混有少量B时,由于A的溶解度受温度的影响较大,而B的溶解度受温度的影响不大,因此可以通过降温结晶或冷却热饱和溶液的方法从它的溶液中得到晶体。
