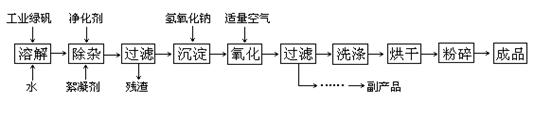
(14分) 复印机使用的墨粉主要成分是Fe3O4,下图是氧化沉淀法生产Fe3O4的工艺:
已知:①工业绿矾中FeSO4的含量为52.5%,其中的杂质不参与反应;
② Fe(OH)2+2Fe(OH)3=Fe3O4·4H2O
③ 12.16﹡1000﹡52.5%=6384,6384/152=42请回答下列问题:
(1)铁的常见氧化物有 ;
(2)Fe3O4与稀硝酸反应的离子方程式是 ,检验反应后的溶液中含Fe3+的方法 ;
(3)在工艺流程中,通入适量空气“氧化”时的化学方程式是: ;
(4)生产中可获得的副产品是 ,提取该副产品的操作顺序是 (填写序号)
a.过滤 b.加热浓缩 c.冷却 d.结晶 e.洗涤
(5)在生产过程中,若工业绿矾的投料速率是12.16 kg/h,为使产品较纯,鼓入空气的速率应为 L/h(假设反应在标准状态下进行,空气中O2占20%)。
(1)FeO、Fe2O3、Fe3O4 (3分)
(2)3Fe3O4 + 28H++NO3-=9Fe3++NO↑+14H2O (2分) 取待测液少许于试管中,加入适量的KSCN溶液,若溶液显血红色,则证明含Fe3+ (2分)
(3)4Fe(OH)2+2H2O+O2=4Fe(OH)3 (2分)
(4)Na2SO4·10H2O(或芒硝,写Na2SO4也可) (1分) bcdae (2分)
(5)784 (2分)
(1)铁的主要化合价是+2价和+3价,所以常见氧化物是FeO、Fe2O3、Fe3O4。
(2)硝酸具有强氧化性,Fe3O4中含有亚铁离子,所以二者发生氧化还原反应,生成硝酸铁和NO及水。检验铁离子一般用KSCN溶液,现象是溶液显血红色。
(3)氢氧化亚铁具有还原性,极易被氧化生成氢氧化铁。
(4)根据转化示意图和原子守恒可判断,副产物是硫酸钠。要使溶液中的硫酸钠析出,需要加热浓缩,然后利用溶解度随温度的变化通过冷却结晶,即得到硫酸钠晶体,过滤洗涤即可。
(5)要使产品较纯,则氧气和氢氧化亚铁要恰好反应。根据题意可知,每小时通过的硫酸亚铁是42mol。根据Fe(OH)2+2Fe(OH)3=Fe3O4·4H2O可知,氢氧化亚铁和氢氧化铁的物质的量之比是1︰2的,所以需要氧化氢氧化亚铁是28mol,则消耗氧气是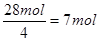 。所以通过的空气是7mol×5×22.4L/mol=784L。
。所以通过的空气是7mol×5×22.4L/mol=784L。
