碳酸钠是造纸、玻璃、纺织、制革等行业的重要原料。工业碳酸钠(钝度约98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO42-等杂质,提纯工艺路线如下
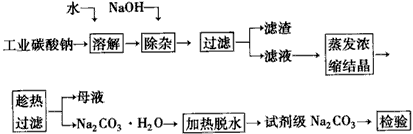
已知碳酸钠的溶解度(S)随温度变化的曲线如下图所示

回答下列问题
(1)滤渣的主要成分为_____________
(2)“趁热过滤”的原因是___________。
(3)若在实验室进行“趁热过滤”,可采取的措施是___________(写出一种)
(4)若“母液”循环使用,可能出现的问题及其原因是______________________。
(5)已知:
Na2CO3·10H2O(s)=Na2CO3(s)+10H2O(g) ΔH1=+532.36 kJ·mol-1
Na2CO3·10H2O(s)=Na2CO3·H2O(s)+9H2O(g) ΔH2=+473.63 kJ·mol-1
写出Na2CO3·H2O脱水反应的热化学方程式______________________。
(1)Mg(OH)2、Fe(OH)3、CaCO3
(2)使析出的晶体为Na2CO3·H2O,防止因温度过低而析出Na2CO3·10H2O晶体或Na2CO3·7H2O晶体,使后续的加热脱水耗时长
(3)用预热过滤装置(或已预热的布氏漏斗趁热抽滤,或用常压热过滤漏斗进行过滤)
(4)产品纯度降低,因为循环使用时母液中Cl-与SO42-浓度增大,导致产品含有NaCl或Na2SO4杂质。
(5)Na2CO3·H2O(s)== Na2CO3(s)+ H2O(g) △H= +58.73kJ/mol

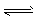 H++A2- 。
H++A2- 。