(1)下 * * 种物质中①Ar、②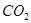 、③
、③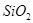 、④NaOH、⑤
、④NaOH、⑤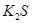 ,只存在共价键的是 (填序号,下同),只存在离子键的是 ,既存在离子键又存在共价键的是 ,不存在化学键的是 。
,只存在共价键的是 (填序号,下同),只存在离子键的是 ,既存在离子键又存在共价键的是 ,不存在化学键的是 。
(2)在以下过程中:①碘的升华、②烧碱熔化、③氯化铵受热分解、④石英熔化、⑤氯化钠溶于水、⑥氯化氢溶于水、⑦氧化钠溶于水、⑧碘溶于四氯化碳,未发生化学键破坏的是
(填序号,下同),仅发生离子键破坏的是 ,仅发生共价键破坏的是 ,既发生离子键破坏、又发生共价键破坏的是 。
(8分)(1) ②③; ⑤; ④;① (2)①⑧ ;②⑤; ④⑥; ③⑦ (各1分)
题目分析:(1)一般活泼的金属和活泼的非金属容易形成离子键,非金属元素的原子间容易形成共价键。据此可知,CO2、二氧化硅中中只有共价键,氢氧化钠中还原离子键和共价键,硫化钾中还原离子键。由于稀有气体元素的最外层电子已经达到稳定结构,所以Ar中不存在化学键。
(2)碘升华、碘溶于四氯化碳是物理变化,破坏的分子间作用力。烧碱是离子化合物,熔化破坏的是离子键。氯化铵受热分解生成氨气和氯化氢,破坏的是离子键和共价键。石英熔化破坏的是共价键。氯化钠是离子化合物,溶于水电离出离子,破坏的是离子键。氯化氢是共价化合物,溶于水破坏的共价键。氧化钠溶于水生成氢氧化钠,破坏的是离子键。
点评:该题是中等难度的是试题,主要是考查学生对化学键含义以及物质变化过程中化学键变化的熟悉了解程度,旨在培养学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑推理能力和抽象思维能力。该题的关键是明确离子键和共价键的含义以及判断依据、形成条件,熔化灵活运用即可。
