氮是地球上含量丰富的原子元素,氮及其化合物在工农业生产、生活中有着重要作用。
(1)25℃时,0.1mol/LNH4NO3溶液中水的电离程度 (填“大于”、“等于”或“小于”) 0.1mol/L NaOH溶液中水的电离程度。
(2)若将0.1mol/L NaOH溶液和0.2mol/LNH4NO3溶液等体积混合,混合溶液中2c(NH4+)>c(NO3-),所得溶液中离子浓度由大到小的顺序是 。
(3)发射火箭时肼(N2H4)为燃料,二氧化氮作氧化剂,两者反应生成氮气和气态水。经测定16g气体在上述反应中放出284kJ的热量。则该反应的热化学方程式是 。
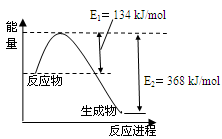
(4)下图是1mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图。
已知:N2(g)+O2(g)=2NO(g) △H=+180kJ/mol
2NO (g)+O2(g)=2NO2(g) △H=-112.3kJ/mol
则反应:2NO(g)+2CO(g) N2(g)+2CO2(g)的△H是 。
N2(g)+2CO2(g)的△H是 。
(1)大于 (2)c(NO3-)>c(NH4+)>c(Na+)>c(OH-)>c(H+)
(3)2N2H4(g)+2NO2(g)=3N2(g)+2H2O (g) △H=-1136kJ/mol(4)-760.3kJ/mol
题目分析: (1)酸、碱抑制水的电离、能水解的盐促进水的电离。
(2)0.1mol/L NaOH溶液和0.2mol/LNH4NO3溶液等体积混合后c(Na+)=0.05mol/L、c(NO3-)=0.1mol/L,由2c(NH4+)>c(NO3-)得c(NH4+)>0.05mol/L。电荷守恒式为c(Na+)+c(NH4+)+c(H+)=c(NO3-)+c(OH-),由c(Na+)、c(NO3-)、c(NH4+)得c(OH-)>c(H+)。所以c(NO3-)>c(NH4+)>c(Na+)>c(OH-)>c(H+)。
(3)2N2H4+2NO2=3N2+2H2O,16gN2H4为0.5mol,所以2molN2H4反应放热1136kJ。
(4)由图像可得NO2(g)+CO(g) CO2(g)+NO(g) △H=-234kJ/mol。由盖斯定律得2NO(g)+2CO(g)
CO2(g)+NO(g) △H=-234kJ/mol。由盖斯定律得2NO(g)+2CO(g) N2(g)+2CO2(g)的△H=-(234×2+180+112.3)kJ/mol=-760.3kJ/mol。
N2(g)+2CO2(g)的△H=-(234×2+180+112.3)kJ/mol=-760.3kJ/mol。
