(5分) 20℃时,将等质量的甲、乙两种固体物质,分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1,加热到50℃时现象如图2,甲、乙两种物质的溶解度曲线如图3。请结合图示回答下列问题:
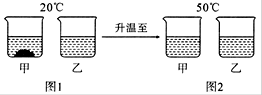
(1)图1中可能为饱和溶液的是 。
(2)图2中甲、乙两溶液中溶质质量分数的大小关系为 。
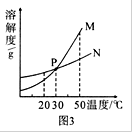
(3)图3中表示乙的溶解度曲线是 ;P点表示的含义是 。
(4)50℃时,将甲物质的不饱和溶液变为饱和溶液,可采取的方法是 。(填三种方法,用分号隔开)
(1)乙 (2)相等或甲=乙 (3)N 30℃时,甲、乙两种固体物质的溶解度相等
(4)降温 加溶质 蒸发溶剂
题目分析:(1)根据饱和溶液的定义结合图示分析,由于甲仍有部分未溶解,则说明甲形成的溶液肯定为饱和溶液,故乙可能为饱和溶液。
(2)图2中,由于甲乙均全部溶解,即为相同质量的溶剂溶解了相同质量的溶质,根据溶质质量分数的计算公式可知,其溶质质量分数相等。
(3)根据图1中信息可知,20℃时,甲的溶解度小于乙的溶解度,而图3中,20℃时,N曲线的溶解度大于M曲线的溶解度,故N表示的是乙物质的溶解度曲线;P点为30℃时,M、N曲线的交点,根据溶解度曲线的意义可知,P点表示30℃时,甲、乙两种固体物质的溶解度相等。
(4)根据溶解度曲线可知,甲物质的溶解度随温度的升高而增大,故50℃时,将甲物质的不饱和溶液变为饱和溶液,可采取的方法是降温、加溶质、蒸发溶剂。
点评:理解和熟记固体溶解度曲线及其使用,了解固体溶解度的概念和意义,掌握溶质质量分数及其有关计算方法,以及饱和溶液和不饱和溶液的概念及其相互转变方法,是解答此类题的关键。
