问题
选择题
已知:H2(g)+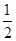 O2(g)=H2O(l) ΔH1=-285.8 kJ·mol-1 ①
O2(g)=H2O(l) ΔH1=-285.8 kJ·mol-1 ①
H2(g)=H2(l) ΔH2=-0.92 kJ·mol-1 ② O2(g)=O2(l) ΔH3=-6.84 kJ·mol-1 ③
H2O(g)=H2O(l) ΔH4=-44 kJ·mol-1 ④
下列说法正确的是
A.上述四个反应都是吸热反应
B.1 mol液态H2的能量大于1 mol气态H2的能量
C.H2的燃烧热(ΔH)为-285.8 kJ·mol-1
D.火箭中液氢燃烧的热化学方程式为H2(l)+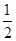 O2(l)=H2O(g) ΔH=-285.8 kJ·mol-1
O2(l)=H2O(g) ΔH=-285.8 kJ·mol-1
答案
答案:C
题目分析:A.②③④是物质状态的变化,没有新物质生成,是物理变化。错误。B.物质由液态转变为气态需要吸收热量,因此1 mol液态H2的能量小于1 mol气态H2的能量。错误。C. 燃烧热是1mol的物质完全燃烧产生稳定的化合物时所放出的热量。液态的水是稳定状态。因此正确。D.①-②×1/2-③-④,整理可得:H2(l)+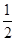 O2(l)=H2O(g) ΔH=-237.46kJ·mol-1.错误。
O2(l)=H2O(g) ΔH=-237.46kJ·mol-1.错误。
