问题
填空题
请完成下列各题:
(1)氢负离子H-基态的电子排布式是___________。
(2)下列变化:H-(g)=H(g)+e-吸收的能量为73 kJ/mol,H(g)=H+(g)+e-吸收的能量为1311 kJ/mol,则氢负离子H-的第一电离能为____________。
(3)氢原子能与许多元素化合形成化合物。下图中“●”代表原子序数在1到10之间的原子实(原子实是原子除去价电子后剩余的部分),小黑点“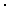 ”代表未成键价电子,短线代表一个化学键。
”代表未成键价电子,短线代表一个化学键。

如H2O表示为: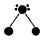
①写出A、B两种分子的立体结构及其中心原子的杂化方式____________,___________。
②C、D与A具有相似的分子结构,且A、C、D三种分子的中心原子属于同族非金属,试推测由A、C、D构成的三种纯净物中沸点最高的是______(填“A”、“C”或“D”),原因是__________________。
答案
(1)1s2
(2)73kJ·mol-1
(3)①sp3;sp2;②A;A的沸点最高,A中存在氢键,C、D中不存在氢键
