海水是种宝贵资源。
(1)“海水晒盐”所采用的方法是 (填写编号)。
I.冷却结晶 II.蒸发结晶 III.过滤
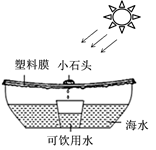
(2)海上航行缺乏饮用水时可采用下图装置获得淡水。用该装置将2000g含氯化钠3%的海水暴晒4小时后, 剩余海水中氯化钠的质量分数为4%,则收集到的可饮用水为 g。
(3)海水中的硼酸(化学式为H3BO3)可用于玻璃工业,下表为硼酸的部分溶解度数据。
| 温度(℃) | 0 | 20 | 40 | 60 | 80 |
| 溶解度(g/100g水) | 3 | 5 | 9 | 15 | 23 |
I.由表可知,硼酸的溶解度随着温度的升高而 (填“增大”或“减小”或“不变”)。
II.60℃时,100g硼酸饱和溶液中含有硼酸 g(保留整数)。
III.某同学设计如下实验探究“温度”及“固体溶质的形态”对溶解速率的影响。
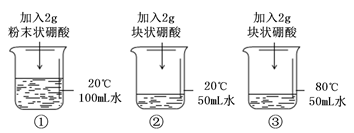
a.上述三个烧杯中,所得溶液浓度的大小关系是 (用“①”、“②”、“③”表示);。b.若要达到实验目的,需改变实验①中的一个条件是 (从以下选项中选择)
A.将20℃的水改为80℃ B.将水的体积改为50mL C.将粉末状固体改为块状
(1)Ⅱ
(2)500
(3)增大,13,②=③﹥①,B
题目分析:(1)“海水晒盐”所采用的方法是蒸发结晶;
(2)该装置实际是采用蒸发的方法,在蒸发过程中,溶质氯化钠的质量不变,故氯化钠的质量
=2000g×3%=60g,那么蒸发后溶液的质量=60g/x =4%,x=1500g,蒸发的水的质量=2000g-1500g=500g;
(3)由表可知,硼酸的溶解度随着温度的升高而增大;60℃时,硼酸的溶解度为15g,即100g水中溶解15g达到饱和状态,那么100g硼酸饱和溶液中含有硼酸的质量为13g;20℃硼酸的溶解度为5g,那么①得到的是不饱和溶液,②与③得到的溶液溶质和溶剂的质量相等,溶质的质量分数相同;探究“温度”及“固体溶质的形态”对溶解速率的影响要采用变用控制变量方法,即溶剂的质量要相等。
