下表是Ca(OH)2和NaOH的溶解度数据。请回答下列问题:
| 温度/℃ | 0 | 20 | 40 | 80 | 100 | |
| 溶解度/ g/100g水 | Ca(OH)2 | 0.173 | 0.165 | 0.121 | 0.094 | 0.076 |
| NaOH | 31 | 91 | 111 | 313 | 336 | |
①从上表数据可以看出,氢氧化钙的溶解度随温度的升高而 。
②40℃时,将20g水配成氢氧化钠饱和溶液,需氢氧化钠的质量为 克。若将40℃时422克的氢氧化钠饱和溶液稀释为20%的溶液,需加水⒁克。
③80℃时含有Ca(OH)2和NaOH两种溶质的饱和溶液,若要从中得到较纯净的NaOH晶体,应采取的物理方法是 。
④现有20℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量CaO后得到的溶液(乙溶液), 此时甲乙两杯溶液中 。
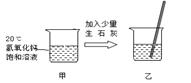
A.甲的溶质的质量分数与乙的相同
B.甲的溶质的质量分数大于乙的
C.甲的溶质的质量小于乙的
D.甲、乙都是饱和溶液
① 减小 ② 22.2 688 ③ 降温结晶并过滤 ④ BD
题目分析:①从上表数据可以看出,氢氧化钙的溶解度随温度的升高而减小
②从上表数据可以查出,40℃时,氢氧化钠的溶解度为111克,意思是在100g水中达到饱和状态溶解的氢氧化钠质量为111克,所以20g水配成氢氧化钠饱和溶液,需氢氧化钠的质量为22.2克,40℃时422克的氢氧化钠饱和溶液中所含的氢氧化钠质量=422克×111克/211克=222克,稀释为20%的溶液时,溶质的质量不变,所以此时溶液的质量=222克÷20%=1110克,所以需加水的质量=1110克-422克=688克
③80℃时含有Ca(OH)2和NaOH两种溶质的饱和溶液,若要从中得到较纯净的NaOH晶体,NaOH的溶解度岁温度的升高而增大,所以应采取的物理方法是:降温结晶并过滤
④在20℃时Ca(OH)2的饱和溶液(甲溶液),加入一定量CaO,CaO会与溶液中的水反应,等于饱和溶液蒸发水分,会析出晶体,同时反应放热,使溶解度降低,所以溶质的质量分数也跟着降低,故A、C错,B正确,析出晶体后的溶液是饱和溶液,D 正确
