(8分)如图(甲)是A、B、C三种固体物质的溶解度曲线图。回答下列问题:
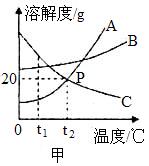
(1)曲线上的P点表示的意义为______________________________;
(2)t2℃时,在50g水中加入20gA物质充分溶解,所得溶液中物质与溶液的质量比为________________。
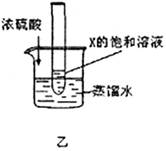
(3)如下图(乙)所示,往常温下的蒸馏水中慢慢加入浓硫酸,结果发现试管内的溶液中出现晶体。则X应该是A、B、C三种物质中的______________。
(4)t1℃时,将A、B、C三物质的饱和溶液分别升温到t2℃,所得溶液的溶质质量分数的由大到小的关系是_________________。
(1)当温度为t2℃时,A、C两物质的溶解度相等。 (2)1:6(20:120) (3)C (4)B>C>A
题目分析:(1)曲线上的P点是A和C的交点,对应的温度为t2℃;所以表示的意义为当温度为t2℃时,A、C两物质的溶解度相等。
(2)t2℃时,A的溶解度为20g。即在t2℃时在100g水中溶解20gA可达到饱和。因此在50g水中加入最多溶解10gA物质;所得溶液中物质与溶液的质量比为10g :(10g +50g)=1:6。
(3)浓硫酸溶解于水时会放出大量的热。即乙中烧杯的温度会升高。“发现试管内的溶液中出现晶体”说明X固体在温度升高时会从其饱和溶液中析出。所以可知X的溶解度会随着温度的升高而降低,则X为C。
(4)t1℃升温到t2℃时,AB的溶解度均变大,不会析出固体。所以其溶液中的质量分数仍和t1℃时它们的饱和溶液的质量分数相等,即按t1℃时两物质的溶解度进行计算。C在升温时其溶解度变小,会有固体析出。所以其形成的溶液仍为饱和溶液。其溶液中溶质的质量分数应按C物质在t2℃时溶解度进行计算。根据图示可知,t1℃时B的溶解度大于t2℃时C的溶解度,t2℃时C的溶解度大于t1℃时A的溶解度。所以所得溶液的溶质质量分数的由大到小的关系是B>C>A。
