工业炼铝是用铝土矿(主要成分是Al2O3,还有少量的Fe2O3、SiO2)提取冶炼铝的主要原料氧化铝,然后进行电解。工艺流程如下图:
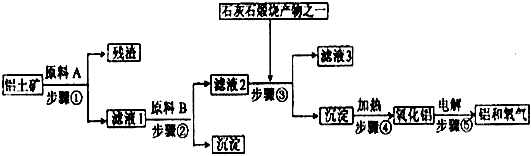
(1)滤液1中要加入稍过量的原料B,原料B的化学式是______________。写出步骤②有关反应的离子方程式_______________________、_________________________。
(2)滤液3中溶质的主要成份是________(填化学式),写出该溶液的一种用途______________________。
(3)如果省去步骤①,即溶解铝土矿从直接加入原料B开始,则最终会对氧化铝的生成有什么影响?
_________________________________。
(4)铝粉与三氧化二铁粉末在引燃剂作用下常用来焊接钢轨,主要是利用了该反应是_____________,而且该反应焊接速度快、设备简易,适于野外作业。
(5)步骤⑤是在铝电解槽中进行,电解槽的两极材料均用石墨,其中___________极的材料随反应的进行需要不断补充,为什么?_____________________________
(1)NaOH;Fe3++3OH-==Fe(OH)3↓;Al3++4OH-==AlO2-+2H2O
(2)NaHCO3;制NaHCO3或发酵粉(答案合理即可)
(3)用NaOH直接溶解会使SiO2生成Na2SiO3,通CO2后生成H4SiO4和Al(OH)3沉淀,从而加热后生成的
Al2O3中混有杂质SiO2
(4)放热反应
(5)阳;阳极生成的O2与石墨反应生成了CO2从而被消耗
