问题
计算题
质量分数不同的硫酸溶液其密度不相同,对照表如下:
| 质量分数 | 10% | 20% | 30% | 40% | 50% | 60% | 70% | 80% | 90% | 98% |
| 密度(g/mL) | 1.07 | 1.14 | 1.22 | 1.30 | 1.40 | 1.50 | 1.61 | 1.73 | 1.81 | 1.84 |
答案
(1)18.0
(2)解:设10mL稀硫酸与锌完全反应消耗锌的质量为x
Zn+H2SO4===ZnSO4+H2↑
65 98
x 18.0g×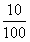
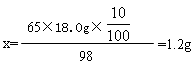
答:消耗金属锌的质量为1.2g
(3)![]() ;b
;b
