化学在能源开发与利用中起着重要的作用,如 甲醇、乙醇、二甲醚(CH3 -O-CH3)等都是新型燃料。
(1)乙醇是重要的化工产品和液体燃料,可以利用下列反应制取乙醇。 2CO2(g)+6H2(g) CH3CH2OH(g) +3H2O(g) △H=akJ.mol-1 在一定压强下,测得上述反应的实验数据如下表。
CH3CH2OH(g) +3H2O(g) △H=akJ.mol-1 在一定压强下,测得上述反应的实验数据如下表。
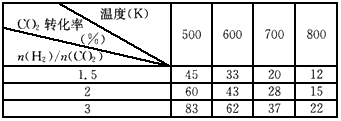
根据表中数据分析:
①上述反应的a____________0(填“大于”或“小于”)。
②在一定温度下,提高氢碳比,则CO2转化率___________(填“增大”“减小” 或“不变”)。
(2)催化剂存在的条件下,在固定容积的密闭容器中投入一定量的CO和H2,同样可制得乙醇(可逆反应)。该反应过程中能量变化如图所示

①写出CO和H2制备乙醇的热化学反应方程式______________
②在一定温度下,2 mol CO(g)和4 mol H2 (g)反应达到平衡时,生成b mol CH3CH2OH(g)和b mol H2O(g),若向上述密闭容器中加入4 mol CO、8 mol H2 及固体催化剂,使之反应。平衡时,反应产生的热量Q__________2E2(填“>”“<” 或“=”);生成CH3CH2OH的物质的量___________2b(填“>”“<”或“=”),你的判 断依据是________________。
(3)二甲醚(CH3OCH3)被称为21世纪的新型燃料,具有清洁、高效的优良性能。 以二甲醚、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池,其工作原理 与甲烷燃料电池原理相类似。该电池中负极上的电极反应式是________________。
(1)①小于 ;②增大
(2)①2CO(g)+4H2(g)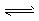 CH3CH2OH(g)+ H2O(g) △H=-E2kJ.mol-1;
CH3CH2OH(g)+ H2O(g) △H=-E2kJ.mol-1;
②< ;> ;容积固定,等比例增加气体反应物的物质的量相当于增大压强,平衡正向移动
(3) CH3OCH3+16OH--12e-=2CO32- + 11H2O
