问题
计算题
向24.8 g硫酸钠和碳酸钠的混合物中滴加硫酸溶液,直到不再产生气体为止(假设气体全部逸出),共用去49 g质量分数为20%的硫酸溶液。求:
(1)原混合物中碳酸钠的质量。
(2)反应后溶液中溶质的质量分数。
答案
解:设原混合物中Na2CO3的质量为x,生成Na2SO4的质量为y,生成CO2的质量为z。
Na2CO3+H2SO4==Na2SO4+H2O+CO2↑
106 98 142 44
x 49g×20%g y z
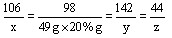
解得 x=10.6 g,y=14.2 g,z=4.4g
原混合物中Na2CO3的质量为10.6 g
原混合物中Na2SO4的质量为24.8 g-10.6 g =14.2 g
反应后溶液中Na2SO4的总质量为14.2 g+14.2 g=28.4 g
反应后溶液的总质量为28.4 g+49 g-4.4 g=73 g
反应后溶液中溶质的质量分数为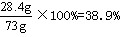
答:原混合物中碳酸钠的质量为10.6 g,反应后溶液中溶质的质量分数为38.9%
