问题
计算题
为了测定一瓶稀硫酸中溶质的质量分数,甲、乙两同学分别没计如下两种方案:
甲:如下图所示(完全反应后锌有剩余)
(1)甲方案需要测量的有: _________ (填序号);
A.反应前锥形瓶、锌和稀硫酸的总质量 B.实验中加入锌的质量
C.完全反应后锥形瓶及其中物质的总质量 D.实验所用稀硫酸的质量
乙:100g稀硫酸 固体A
固体A 固体A为46.6g.
固体A为46.6g.
(2)利用乙方案求此稀硫酸中溶质的质量分数,写出计算过程.

答案
(1)ACD
(2)解:设参加反应的纯硫酸的质量是X克.
H2SO4+BaCl2==2HCl+BaSO4↓
98 233
x 46.6
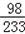 =
=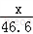
得:X=19.6
稀硫酸中溶质的质量分数=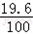 ×100%=19.6%
×100%=19.6%
答:稀硫酸中溶质的质量分数为19.6%.
