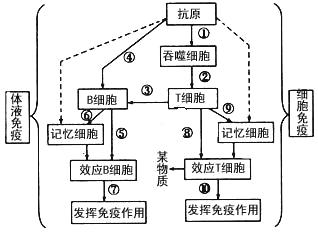
问题
填空题
海水的综合利用可以制备金属镁,其流程如下图所示
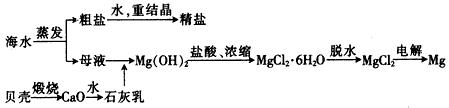
(1)电解MgCl2时,生成Mg的电极是_________(填“阴”或“阳”)极。
(2)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,其中过滤中玻璃棒的作用是_____________。
(3)若在空气中加热MgCl2·6H2O生成的是Mg(OH)Cl或MgO,写出相应反应的化学方程式:_________________________。若要制得无水MgCl2,则需在________中加热MgCl2·6H2O。
(4)Mg(OH)2沉淀中混有的Ca(OH)2应怎样除去?写出涉及的反应的化学方程式:__________________。
答案
(1)阴
(2)引流
(3)MgCl2·6H2O Mg(OH)Cl+HCl↑+5H2O(或MgCl·6H2O
Mg(OH)Cl+HCl↑+5H2O(或MgCl·6H2O MgO+2HCl↑+5H2O);HCl气流
MgO+2HCl↑+5H2O);HCl气流
(4)Ca(OH)2+MgCl2=CaCl2+Mg(OH)2↓