问题
填空题
已知2A2(g) +B2 (g) 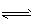 2C3 (g)△H= -Q1kJ·mol-1(Q1>0),在-个有催化剂的固定容积的容器中加入2mol A和1mol B2,在500℃时充分反应,达平衡后C3的浓度为ωmol·L-1,放出热量Q2kJ。
2C3 (g)△H= -Q1kJ·mol-1(Q1>0),在-个有催化剂的固定容积的容器中加入2mol A和1mol B2,在500℃时充分反应,达平衡后C3的浓度为ωmol·L-1,放出热量Q2kJ。
(1)若在原来的容器中,只加入2 mol C3,500℃时充分反应达平衡后,吸收热量 Q3 kJ,C3浓度___(填“>”“=”或“<”)ω mol·L-1,Q1、Q2、Q3之间满足何种关系___(用代数式表示)。
(2)能说明该反应已经达到平衡状态的是___。
a.v(C3)=2v(B2);
b.容器内压强保持不变
c.v逆(A2) =2v正(B2)
d.容器内的密度保持不变
(3)改变某一条件,得到如图的变化规律(图中T 表示温度,n表示物质的量),可得出结论正确的是 ____。
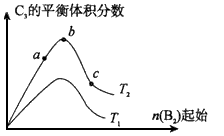
A.反应速率c>b>a
B.达到平衡时A2的转化率大小为:b>a>c
C.T2 >T1
D.b点时,平衡体系中A、B原子数之比接近2:1
(4)若将上述容器改为恒压容器(反应前体积相同),起始时加入2 mol A2和 1 molB2,500℃时充分反应达到平衡后,放出热量Q4 kJ,则Q2____Q4(填 “>”“=”或“<”),理由是___。
答案
(1)= ;Q1=Q2+Q3
(2)bc
(3)AD
(4)< ;恒压条件下,由于始终保持较大压强,故反 应转化率较高,放出热量较多
