我国规定饮用水质量标准必须符合下列要求:
| pH | 6.5~8.5 |
| Ca2+、Mg2+总浓度 | <0.0045mol·L-1 |
| 细菌总数 | <100个/mL |
某综合实践活动小组到自来水厂进行参观,了解到源水处理成自来水的工艺流程示意
图如下: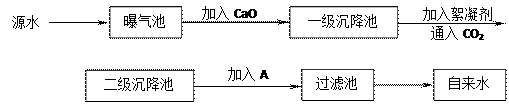
(1)源水中含Ca2+、Mg2+、HCO3-、Cl-等,加入CaO后生成,进而发生若干个化学反应,请写出其中任意一个反应的离子方程式 。
(2)加入絮凝剂可以除去其中的悬浮固体颗粒,该过程是 (填写序号)。
①只有物理过程,无化学过程
②只有化学过程,无物理过程
③既有物理过程,又有化学过程
(3)FeSO4·7H2O是常用的絮凝剂,加入后最终生成红褐色胶状沉淀,则这种沉淀是 (填写化学式)。
(4)通入二氧化碳的目的是 和 。
(5)物质A的作用是 ,则A可以选择下列物质中的 (填写序号)。
①ClO2 ②SO2 ③液氯 ④Ca(ClO2)2 ⑤浓硫酸
(1)HCO3-+OH-====CO32-+H2O Ca2++HCO3-+OH-====CaCO3↓+H2O
Ca2++2HCO3-+2OH-====CaCO3↓+CO32-+2H2O Mg2++2OH-====Mg(OH)2↓
(写出任意一个,即可得2分)
(2)③(1分) (3)Fe(OH)3(1分)
(4)除去钙离子(1分) 调节溶液酸碱度(1分)
(5)杀菌消毒(1分) (6)①③④(3分,每选1个得1分,选错1个倒扣1分)
絮凝剂往往利用其中金属阳离子水解生成的胶体的吸附能力,吸附杂质以达到净水的目的,水解生成胶体的过程是化学变化,吸附杂质的过程属于物理变。 FeSO4·7H2O就水解生成氢氧化亚铁,氢氧化亚铁很容易就被氧化成氢氧化铁胶体。除了沉淀,还要用强氧化剂杀菌消毒,故

 温同压下4.75体积氧气。试回答:
温同压下4.75体积氧气。试回答: 体的结构简式为 。
体的结构简式为 。