问题
填空题
一定温度下,在容积为1L的密闭容器内放入2mol N2O4和8 mol NO2,发生如下反应:
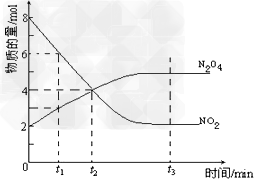
2NO2(红棕色) N2O4(无色)(△H<0),反应中NO2、N2O4的物质的量随反应时间变化的曲线如下图,按下列要求作答
N2O4(无色)(△H<0),反应中NO2、N2O4的物质的量随反应时间变化的曲线如下图,按下列要求作答
(1)在该温度下,反应的化学平衡常数表达式为:_______________
(2)若t1=10s,t2=20s,计算从t1至t2时以N2O4表示的反应速率:_________mol·L-1·s-1
(3)图中t1、t2、t3哪一个时刻表示反应已经达到平衡?____________________
(4)t1时,正反应速率______(填“>”、“<”或“=”)逆反应速率
(5)维持容器的温度不变,若缩小容器的体积,则平衡向______移动 (填“正反应方向”、“逆反应方向”或“不移动”)
(6)维持容器的体积不变,升高温度,达到新平衡时体系的颜色___________(填“变深”、“变浅”或“不变”)
答案
(1)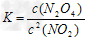
(2)0.1
(3)t3
(4)>
(5)正反应应方向
(6)变深
