过氧化氢(H2O2)的水溶液俗称双氧水,其水溶液可用于制备工业上的漂白剂、特殊环境里燃料燃烧的助燃剂、医疗上的消毒剂、实验室里的制氧剂;过氧化钠(Na2O2)可用于制备工业上的漂白剂、特殊环境里的供氧剂、实验室里的制氧剂。过氧原子团“O2”由2个氧原子共用1对电子组成。
(1)分别写出H2O、Na2O2的电子式:_______、________。
(2)①H2O、H2O2中化学键的不同点是_________________;
②Na2O、Na2O2中化学键的不同点是_________________;
③H2O2、Na2O2的化合物类型是(共价化合物、离子化合物)__________________。
(3)分别写出H2O2、Na2O2作供氧剂的化学反应方程式
H2O2:___________________;Na2O2:_______________________。
(4)H2O2与Na2O2相比,化学键更稳定的是(写物质的名称)_______,主要根据是___________________________。
(1)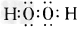 ;
;
(2)①H2O中没有非极性键,H2O2中有非极性键; ②Na2O中没有共价键,Na2O2中有共价键(或非极性键) ;③H2O2是共价化合物,Na2O2是离子化合物
(3)2H2O2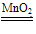 2H2O+O2↑;2Na2O2+2H2O=4NaOH+O2↑或2Na2O2+2CO2= 2Na2CO3+O2
2H2O+O2↑;2Na2O2+2H2O=4NaOH+O2↑或2Na2O2+2CO2= 2Na2CO3+O2
(4)过氧化氢;Na2O2在常温下跟水快速反应生成O2,H2O2的水溶液在催化剂作用下才能较快地反应生成O2
