溶液是生活中常用的混合物.
(1)硫酸铜溶液可用于游泳池消毒,硫酸铜溶液中的溶质是______.
(2)市售的过氧乙酸(CH3COOOH)溶液中溶质的质量分数大多为40%,稳定性差,室温下就可分解成乙酸(CH3COOH),并释放出氧气,该反应的化学方程式为______.将40% 的过氧乙酸溶液稀释成2%,可用于空气消毒,稀释过程中浓溶液与所加水的质量比为______.
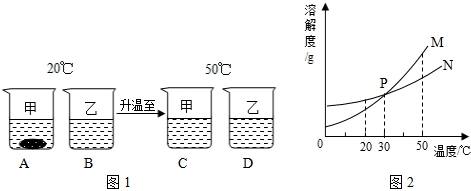
(3)甲、乙两种固体物质的溶解度曲线如图2所示.20°C时,将等质量的甲、乙分别放入盛有100g水的烧杯中,充分搅拌并升温至50°C时,实验现象如图1所示.请结合图示回答下列问题:
①曲线N表示______(填“甲”或“乙”)的溶解度随温度变化的情况.
②图1所示的四种溶液中,溶质质量分数最小的是______(填字母序号,下同),一定不饱和的是______.
(1)硫酸铜溶液是硫酸铜固体溶于水形成的溶液,只要有水,水一定是溶剂,所以硫酸铜是溶质;
(2)由题意可知反应物是过氧乙酸写在等号的左边,生成物是乙酸和氧气写在等号的右边,用观察法配平即可,氧气后面标上上升符号,所以方程式是:2CH3COOOH=2CH3COOH+O2↑;将40% 的过氧乙酸溶液稀释成2%,需要加入水,由于水中没有溶质可看做质量分数为0,根据
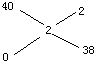
十字交叉法:浓度大的数写在上边,浓度小的数写在下面,混合后的写在中间,大数减小数即可,所以浓度为40%的溶液与水的质量比是2:38=1:19;
(3)①20℃时N的溶解度大于M的,由烧杯AB中的现象可知甲的溶解度小于乙的,所以曲线N表示乙的溶解度曲线;
②由于B、C、D烧杯中加入的溶质、溶剂质量相等,所以溶质质量分数相等,A烧杯中加入的溶质与其它烧杯溶质相等,但是有不溶解的,所以溶质质量少了,所以A烧杯中溶质质量分数最小;A烧杯中有固体不溶物,说明A溶液一定是饱和溶液,B烧杯中没有不溶物,可能不饱和也可能刚好饱和,因为在50℃M、N的溶解度都大于20℃M、N的溶解度,且溶液中含有的溶质和溶剂没变,所以C、D烧杯中的溶液一定是不饱和溶液.
故答案为:(1)硫酸铜(或CuSO4);(2)2CH3COOOH=2CH3COOH+O2↑;1:19;(3)①乙;②A;CD.
