长期以来一直认为氟的含氧酸不存在.但是至1971年斯图杰尔和阿佩里曼(美)成功地合成了次氟酸后,这种论点被剧烈地动摇了.他们是在0℃以下将氟化物从细冰末的上面通过,得到毫克量的次氟酸.
(1)以下两种结构式,能正确表示次氟酸结构的是______.A、H-O-F B、H-F-O
(2)次氟酸中氧元素的化合价为______,次氟酸的电子式为______,次氟酸分子中共价键的键角______180°(填“<”或“=”).
(3)下面给出了几个分子和基团化学键的键能:
| H2 | O2 | F2 | OH | OF | HF | |
| E/(kJ/mol) | 432 | 494 | 155 | 424 | 220 | 566 |
(4)次氟酸能被热水瞬间分解,生成一种常见的物质M,M是18e-,且被称为“绿色氧化剂”.写出次氟酸与热水反应的化学方程式:______.
(1)因HFO为共价化合物,根据共价键成键的特点,氢原子形成一对共用电子对,氧原子形成两对共用电子对,氟原子形成一对共用电子对,其结构式为H-O-F,故答案为:A;
(2)因为F元素吸引电子对的能力比O元素强,在次氟酸中F元素呈-1价,H元素为+1价,则O元素呈零价,次氟酸的电子式
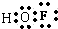
,次氟酸中心原子是氧,采用sp3杂化,分子中共价键的键角<180°,
故答案为:0;
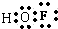
;<;
(3)反应热=反应物的总键能-生成物的总键能=424KJ/mol×2+220 KJ/mol×2-566KJ/mol×2-494KJ/mol=-338KJ/mol,次氟酸分解放出大量的热,故有强氧化性,故答案为:-338;具有强氧化性;
(4)被称为“绿色氧化剂”的过氧化氢(H2O2),次氟酸与热水反应的化学方程式:HOF+H2O=△=HF+H2O2,
故答案为:HOF+H2O=△=HF+H2O2;
