(12分)⑴铁钉在氯气中被锈蚀为棕黄色物质FeCl3,而在盐酸中却生成浅绿色的FeCl2溶液。则在Cl2、Cl-、H+中,具有氧化性的是___________,其中氧化性最强的是_______。
⑵盐酸在不同的反应中,可以分别表现出酸性、氧化性和还原性。现有如下三个反应,请指出盐酸在三个反应中所分别表现的性质:
①Zn+2HCl=ZnCl2+H2↑ ______________________________
②Fe2O3+6HCl=2FeCl3+2H2O ______________________________
③2HCl H2↑+Cl2↑ ______________________________
H2↑+Cl2↑ ______________________________
⑶找出⑵小题中属于氧化还原反应的化学方程式并标出电子转移的方向和数目。
:⑴Cl2、H+(2分) Cl2
⑵①酸性、氧化性(1分) ②酸性(1分) ③既表现氧化性又表现还原性(1分)
⑶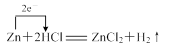 或
或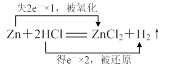 (2分)
(2分)
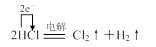 或
或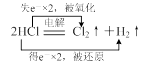 (2分)
(2分)
题目分析:(1)Cl2、H+化合价能降低,所以具有氧化性。其中Cl2是强氧化性物质。
(2)①反应HCl中H化合价降低做氧化剂具有氧化性,同时生成盐ZnCl2体现了HCl的酸性。
②不属于氧化还原反应,HCl只体现酸性。
③HCl中的化合价既有升高又有降低,所以既表现氧化性又表现还原性。
点评:熟练掌握氧化还原反应的基本概念。
