A、B、X、Y和Z是原子序数依次递增的短周期元素,其中A与Y同主族,X与Z同主族,A与B和A与X均可形成10个电子化合物;B与Z的最外层电子数之比为2:3,常见化合物Y2X2与水反应生成X的单质,其溶液可使酚酞试液变红.请回答下列问题.
(1)Z的原子结构示意图为______;化合物BA4的电子式为______.
(2)化合物Y2X2中含有的化学键类型有______(填序号).
A.离子键 B.极性共价键 C.非极性共价键 D.氢键
(3)化合物A2X和A2Z中,沸点较高的是______(填化学式),其主要原因______.
(4)A与X和A与Z均能形成18个电子的化合物,此两种化合物发生反应的化学方程式为______.
A与B和A与X均可形成10个电子化合物,则A应为H元素,A与Y同主族,则Y为Na元素,常见化合物Y2X2与水反应生成X的单质,其溶液可使酚酞试液变红,则X为O元素,Y2X2为Na2O2,X与Z同主族,则Z为S元素,B与Z的最外层电子数之比为2:3,则B元素的最外层电子数为4,根据A、B、X、Y和Z是原子序数依次递增的短周期元素,B应为C元素,
(1)Z为S元素,核电核数为16,原子核外有3个电子层,最外层电子数为6,则原子结构示意图为
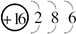
,
化合物BA4为CH4,为共价化合物,电子式为
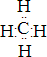
,故答案为:
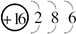
,
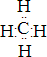
;
(2)Y2X2为Na2O2,为离子化合物,化合物中含有过氧键,氧原子之间为非极性共价键,故答案为:AC;
(3)O原子半径较小,非金属性较强,H2O存在氢键,沸点在同主族元素中形成的氢化物最高,
故答案为:H2O;H2O中存在氢键;
(4)A与X和A与Z均能形成18个电子的化合物,这两种化合物分别为H2O2和H2S,H2O2具有氧化性,H2S具有还原性,二者发生氧化还原反应生成H2O和S,
反应的方程式为H2O2+H2S═2H2O+S↓,故答案为:H2O2+H2S═2H2O+S↓.
