问题
选择题
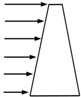
如图所示,一束白光从左侧射人肥皂薄膜,下列说法中正确的是( )
①人从右侧向左看,可看到彩色条纹
②人从左侧向右看,可看到彩色条纹
③彩色条纹水平排列
④彩色条纹竖直排列.
A.②③
B.①②④
C.②④
D.①③
答案
前后表面的反射光在前表面发生叠加,所以在薄膜的左侧出现条纹,由于各种色光的波长不一样,所以在薄膜的左侧出现彩色条纹.因为路程差即(膜的厚度的两倍)是半波长的偶数倍,振动加强,为亮条纹,路程差是半波长的奇数倍,振动减弱,为暗条纹.所以出现亮条纹时,膜的厚度相同,则彩色条纹水平排列.故②、③正确,①、④错误.
故选:A.
